 15/12/2021
15/12/2021
Detectados dos nuevos compuestos que inhiben al gen Ras y muestran menos toxicidad
Detectados dos nuevos compuestos que inhiben al gen Ras y muestran menos toxicidad
- Investigadores del equipo dirigido por Eugenio Santos, investigador principal del Centro de Investigación del Cáncer (CIC-IBMCC; Universidad de Salamanca-CSIC), y jefe de grupo del CIBER de Cáncer (CIBERONC) han comprobado la viabilidad de dos compuestos para que sean empleados en el diseño de nuevos fármacos dirigidos a inhibir al gen Ras.
Todas las proteínas de Ras son GTPasas y están implicadas en procesos críticos de la vida de las células como son el ciclo celular, la migración, los cambios del citoesqueleto, la apoptosis y la senescencia. El gen Ras se encuentra mutado en el 30% de los cánceres, por tanto, la búsqueda de nuevos fármacos dirigidos a este gen es crucial para mejorar tratamiento de muchos de ellos.
Antes de iniciar un ensayo clínico con humanos, se deben realizar investigaciones preclínicas con modelos animales para corroborar la eficacia de los fármacos investigados no sólo para que revierta los efectos de la patología, sino también para evitar efectos secundarios graves, como por ejemplo la toxicidad del producto en el organismo. Si no se superan estas fases de experimentación, en ensayo clínico en personas no se inicia. En este contexto, investigadores del grupo dirigido por Eugenio Santos, han realizado una búsqueda para aislar compuestos que pueden ser empleados en nuevas terapias contra el cáncer. En concreto, han buscado inhibidores de la activación de las GTPasas Ras por su activador GEF SOS1. El análisis se ha llevado a cabo porque estas GTPasas regulan procesos proliferativos en la célula y se ha constatado que están mutadas en numerosos tipos de cáncer.
Alberto Fernández Medarde, Rocío Fuentes Mateos, Rósula García Navas y Andrea Olarte San Juan, del grupo de Eugenio Santos han realizado, dentro del programa “Mecanismos de progresión tumoral”, una búsqueda para aislar compuestos con capacidad de inhibir la activación de las GTPasas Ras por su activador GEF SOS1. La investigación se ha llevado a cabo mediante el análisis de dos colecciones, una cedida por el Instituto Nacional de la Salud de Estados Unidos (NIH) y la segunda por la compañía biotecnológica Biomar Microbial Technologies. La colección cedida por el NIH pertenece al programa de búsquedas de nuevos usos para moléculas ya comercializadas, mientras que la segunda colección está integrada por compuestos de origen marino, que no han sido probados ni utilizados previamente de manera comercial.
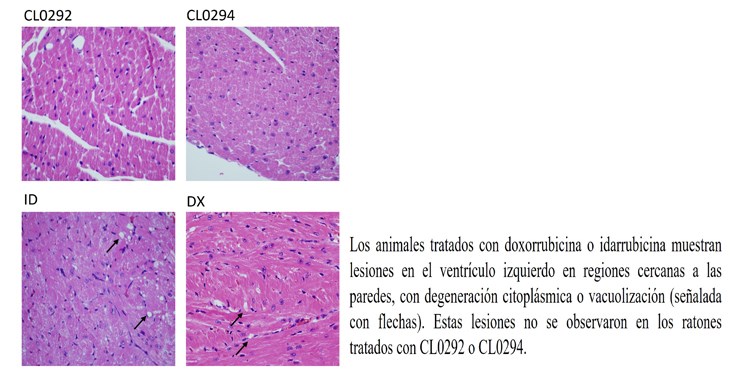
Mediante el análisis se han seleccionado cuatro compuestos por su actividad inhibitoria de la activación de Ras por SOS1 y todos ellos pertenecen a la misma familia de moléculas, conocida como antraquinonas. Esta familia ya ha sido empleada en otras ocasiones en terapias contra el cáncer, sin embargo, mediante este análisis se ha comprobado una función nueva de esta familia que permitirá continuar con la investigación de nuevas terapias. De las cuatro antraquinonas seleccionadas se han descartado dos de ellas (denominadas Idarrubicina y Doxorrubicina) porque se demostrado que produce muchos efectos secundarios que impiden su desarrollo, se ha detectado una alta cardiotoxicidad en ratones. Sin embargo, los dos compuestos aislados de la colección de Biomar Microbial Technologies no han mostraron toxicidad con las dosis empleadas.
Gracias a los resultados obtenidos, se abre una nueva vía para el desarrollo de antraquinonas más activas en la inhibición de la activación de Ras y que son menos tóxicas para los pacientes.
Referencia del artículo:
Fernández-Medarde A, Fuentes-Mateos R, García-Navas R, Juan AO, Sánchez-López JM, Fernández-Medarde A, Santos E. Anthraquinones as Inhibitors of SOS RAS-GEF Activity. Biomolecules. 2021 Jul 30;11(8):1128. doi: 10.3390/biom11081128. PMID: 34439794; PMCID: PMC8392861.
Foto del laboratorio Eugenio Santos:
www.cicancer.org/media/1888/eugeniosantos_lab.jpg
Más información.
Difusión CIBER de cáncer: https://www.ciberonc.es/
Difusión de la Universidad de Salamanca: https://saladeprensa.usal.es/node/129717





